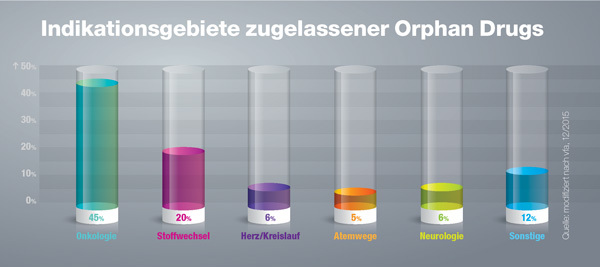
Seit dem Jahr 2000 enzwickeln forschende Pharmaunternehmen verstärkt Medikamente gegen seltene Erkrankungen. Für diese Mediakamente gelten ein paar rechtliche Besonderheiten über die Birgit Fischer im Interview aufklärt.

Birgit Fischer
Hauptgeschäftsführerin des Verbands forschender Arzneimittelhersteller
Wann erhält ein Medikament den Status als „Orphan Drug“?
Der Orphan-Drug-Status gilt ausschließlich für Medikamente gegen Krankheiten, an denen weniger als fünf von 10.000 EU-Bürgern leiden.
Der Status ist mit einer Unterstützung der EU-Arzneimittelbehörde bei der Erprobung der Medikamente in Studien, mit Gebührennachlässen und mit einem zehnjährigen Schutz vor ähnlichen Konkurrenzpräparaten verbunden.
Er soll Unternehmen motivieren, mehr dafür zu tun, dass Patienten mit seltenen Erkrankungen keine Waisenkinder der Medizin mehr sind.
Kann der Status auch wieder aberkannt werden?
Ja. Schon bei der Zulassung verliert ein Medikament diesen Status wieder, wenn es keinen Therapiefortschritt bringt. Er verhindert auch nicht, dass ein besseres Medikament auf den Markt kommen kann. Zehn Jahre nach Markteinführung endet der Status zudem regulär.
Im Zusammenhang mit den „Orphan Drugs“ stößt man immer häufiger auf zwei Begriffe: „Orphanisierung“ und „Trojaner“. Was versteht man darunter und wie viel Mythos steckt dahinter?
Es wurde spekuliert, Unternehmen könnten die Orphan-Drug-Vorzüge auch für gewöhnliche Medikamente erlangen, indem sie diese pro forma nur für Unterformen einer häufigeren Krankheit zur Zulassung bringen. So eine „Orphanisierung“ lässt die EU-Arzneimittelbehörde aber gar nicht durchgehen.
Es wurde auch unterstellt, die Unternehmen entwickelten ihre Medikamente zunächst gegen eine seltene Krankheit, um sie dann auch gegen häufigere Krankheiten zu vermarkten. Der Orphan-Status diene quasi als trojanisches Pferd zum Massenmarkt. Auch das ist ein Irrtum.
Denn nur durch neue Studien und Zulassungsverfahren könnte ein Orphan Drug ein solches neues Anwendungsgebiet dazubekommen und müsste zugleich seinen Orphan-Status aufgeben. So ist sichergestellt, dass der Status exklusiv seinem Förderziel dient: der Entwicklung der dringend benötigten neuen Therapien für Patienten mit seltenen Krankheiten.
Autor: